トップページ > 広報活動 > 研究トピックス > 2023年度 > EGFR遺伝子変異陽性早期肺がんに対する術後補助療法としてオシメルチニブが全生存期間の延長を示す
EGFR遺伝子変異陽性早期肺がんに対する術後補助療法としてオシメルチニブが全生存期間の延長を示す-The New England Journal of Medicineに論文発表-
2023年9月4日
国立研究開発法人国立がん研究センター
発表のポイント
- 根治を目的とした完全切除後のEGFR遺伝子変異*1陽性早期非小細胞肺がんを対象とした国際共同第III相試験の結果、術後補助療法において、オシメルチニブ*2が副次評価項目である全生存期間を統計学的かつ臨床的に有意に延長することが示されました。
- 術後補助療法としてゲフィチニブなど従来のEGFR阻害剤では示されていなかった全生存期間の延長が、オシメルチニブによって世界で初めて証明されました。
- 本試験の結果、再発率が高く、術後の治療選択肢が限られていたEGFR遺伝子変異陽性の早期非小細胞肺がん患者さんに対し、エビデンスに基づいた治療提供が可能となります。
- 本試験の成果は2023年米国臨床腫瘍学会 (ASCO) で報告され、また米国学術雑誌「The New England Journal of Medicine」に掲載されました。
概要
国立研究開発法人国立がん研究センター(理事長:中釜 斉、東京都中央区)東病院(病院長:大津 敦、千葉県柏市、以下東病院)では、国民に新しい薬・治療法をいち早く提供することを目指し、治験・臨床研究に積極的に取り組んでいます。
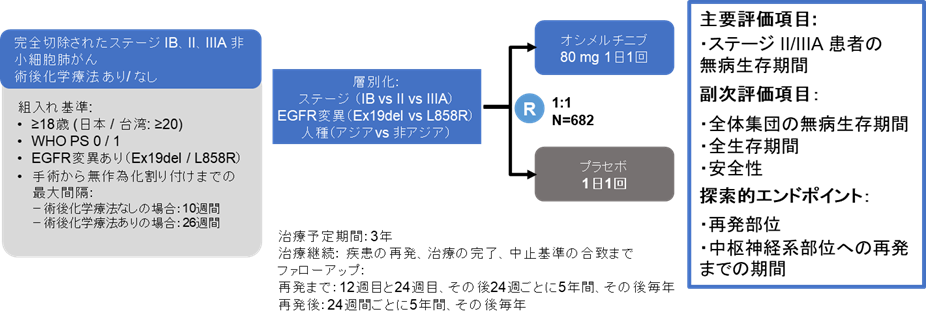
この度東病院では、腫瘍の完全切除後のEGFR(上皮増殖因子受容体)遺伝子変異陽性の非小細胞肺がん患者さん(ステージIB~IIIA期)を対象に、オシメルチニブによる術後補助療法の有効性、安全性を評価する無作為化二重盲検*3プラセボ*4対照の国際共同第III相試験:ADAURA試験(国際調整医師および治験責任医師:国立がん研究センター東病院 呼吸器外科長 坪井 正博)に参加し、これまでに報告されていた主要評価項目である無病生存期間(手術後の再発もしくは死亡までの期間)の延長、改善に加え、重要な副次評価項目である全生存期間(手術後から死亡までの期間)においても、プラセボ群に比べて統計学的に有意かつ臨床的に意義のある改善が示されたことを発表しました。
本試験の成果は2023年米国臨床腫瘍学会 (ASCO)で報告され、また米国学術雑誌「The New England Journal of Medicine」(2023年6月4日付)に掲載されました。
背景
肺がんは日本のみならず世界でも罹患数、死亡数が多いがんです。また、治療が困難な難治がんのひとつであり、治療開発が推進されています。近年、がん検診やCTの普及により、より早期に肺がんが発見される機会が増え、治癒を目指せる1つの治療として手術後に薬物療法を実施する術後補助療法の治験・臨床研究が盛んに行われています。手術を受けた肺がん患者さんの5年生存率はステージIB期で約70%、ステージII期で約60%、ステージIIIA期では約40%であり、更なる改善が強く求められています。
また、最近ではがんの原因となる遺伝子変化を明らかにして、その遺伝子変化に対応する有効性の高い薬物療法の開発も進んでいます。遺伝子変化を明らかにし、手術後に有効性の高い薬物療法を実施することで、5年生存率がさらに改善出来るのではないかと期待されてきました。
研究方法・成果
ADAURA試験は、アストラゼネカのサポートによる企業主導治験です。腫瘍の完全切除後(補助化学療法実施の有無は医師と患者さんの判断)のEGFR遺伝子変異陽性非小細胞肺がん患者さん(ステージIB~IIIA期)を対象に、オシメルチニブの術後補助療法に対する有効性、安全性を評価する無作為化二重盲検プラセボ対照国際共同第III相試験で、患者さんは「プラセボ」あるいは「オシメルチニブ」を経口投与にて3年間または再発するまで治療を受けました。
なお、本試験は米国、欧州、南米、アジア、中東の20カ国以上、200を超える施設から682例が登録されました。
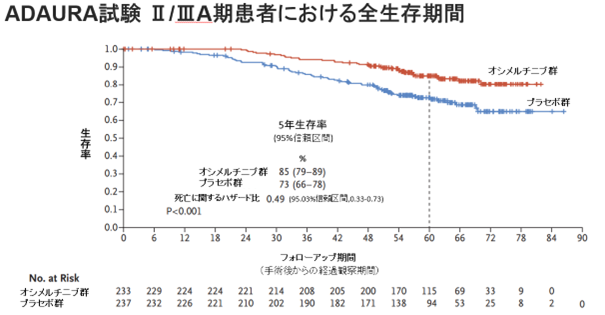
患者さんの最終登録終了後、4年後(観察期間の中央値:60ヵ月超)に全生存期間に関して解析が行われ、ステージII期およびIII期の5年生存率はオシメルチニブ群で85%、プラセボ群で73%であり、術後補助療法としてオシメルチニブを服用していた場合、5年生存率を12%改善することが出来ました。
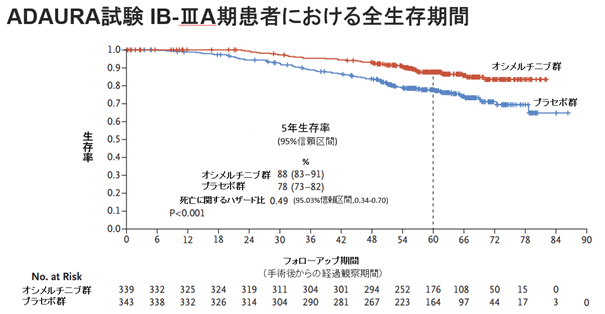
また、ステージIBも含めた5年生存率はオシメルチニブ群で88%、プラセボ群で78%であり、術後補助療法としてオシメルチニブを服用していた場合、5年生存率を10%改善することが出来ました。
以上の結果から、進行・再発期のEGFR遺伝子変異陽性非小細胞肺がんに対応する標準的薬物療法であるオシメルチニブを、手術後に術後補助療法として服用することで、5年生存率がこれまでより改善出来ることが証明されました。また、肺がん治療を選択する際にはEGFR遺伝子変異の有無を確認することが重要であることが裏付けられました。
なお、オシメルチニブの安全性については、これまで報告されていた内容と同じで、新たな懸念はありませんでしたが、日本人の患者さんでは進行期の肺がんで治療する際に認められる薬剤性の肺障害が起こる可能性がありますので、注意を要します。
展望
本試験の結果を受け、再発率が高く、術後の治療選択肢が限られていたEGFR遺伝子変異陽性の早期非小細胞肺がん患者さんの術後補助療法として、オシメルチニブが標準治療として推奨されます。オシメルチニブをさらに早期の再発リスクの高い患者に使えないか、少し進行した肺がんの患者さんの手術前に使用することで治療成績をより改善できないかと、新たな治験を立ち上げて治療開発を進めています。
国立がん研究センター東病院 呼吸器外科、呼吸器内科では、本試験のような国境の垣根を越えて行われている薬物療法や放射線治療と外科手術を併用した治験・臨床研究に積極的に取り組み、早期肺がん患者さんの治療開発を進めてまいります。
発表論文
雑誌名
The New England Journal of Medicine
タイトル
Overall Survival with Osimertinib in Resected EGFR-Mutated NSCLC
著者
Masahiro Tsuboi, M.D., Roy S. Herbst, M.D., Ph.D., Thomas John, M.B., B.S., Ph.D., Terufumi Kato, M.D., Margarita Majem, M.D., Ph.D., Christian Grohé, M.D., Jie Wang, M.D., Ph.D., Jonathan W. Goldman, M.D., Shun Lu, M.D., Wu-Chou Su, M.D., Filippo de Marinis, M.D., Frances A. Shepherd, M.D., Ki Hyeong Lee, M.D., Ph.D., Nhieu Thi Le, M.D., Arunee Dechaphunkul, M.D., Dariusz Kowalski, M.D., Ph.D., Lynne Poole, M.Sc., Ana Bolanos, M.D., Yuri Rukazenkov, M.D., Ph.D., and Yi-Long Wu, M.D. for the ADAURA Investigators
DOI
10.1056/NEJMoa2304594
掲載日
2023年6月4日
URL
https://www.nejm.org/doi/full/10.1056/NEJMoa2304594?query=featured_hematology-oncology
研究費
本試験は、アストラゼネカからの資金提供を受け実施されました。
用語解説
*1 EGFR遺伝子変異
非小細胞肺がんの細胞の表面にはEGFR(上皮成長因子受容体)と呼ばれるタンパク質がたくさん発現しており、このEGFRは外部から刺激を受けると、がん細胞が増え続ける(増殖)のに必要な信号を細胞内に伝える役割を担っている。
EGFR遺伝子変異にはいくつかのパターンがあり、特に発現が多い遺伝子変異は、EGFR遺伝子の中のエクソン19という部位の一部がなくなっている「エクソン19欠失」、エクソン21という部位の塩基の並びが入れ替わっている「L858R点変異」。
*2 オシメルチニブ
EGFRのチロシンキナーゼ部位を阻害することで、がん細胞の増殖を抑えることを目的としたEGFR-TKIとよばれる分子標的治療薬。
*3 無作為化二重盲検
登録された患者さんをランダムに各治療群に割り付けるが、どちらの群に割り付けられたかは患者さんや医師も含め、全ての関係者が患者さんにどのお薬を使用しているかわからない手法。
*4 プラセボ
薬の有効成分を含まない薬。
お問い合わせ先
研究に関するお問い合わせ
国立研究開発法人国立がん研究センター東病院
呼吸器外科 科長 坪井 正博
電話番号:04-7133-1111(代表電話)
Eメール:mtsuboi●east.ncc.go.jp
